Salud y Bienestar
Ángela Nieto (CSIC): “El gran reto es impedir las metástasis del cáncer”
Publicado
hace 5 añosen

La bióloga del CSIC en el Instituto de Neurociencias de Alicante estudia los mecanismos de los procesos embrionarios que se reactivan en la edad adulta y pueden dar lugar a enfermedades como el cáncer
Ángela Nieto lleva más de 25 años observando cómo, cuándo y por qué las células migran de un lugar a otro dentro del organismo. Su trabajo parte de una constatación: “En algunas patologías como el cáncer se produce una reactivación de procesos embrionarios”. Y da otra pista: “Bajo esta premisa, intentamos entender y prevenir la formación de metástasis o reparar órganos dañados”. Aquí aparece el concepto de plasticidad celular, que hace referencia a los cambios de comportamiento de las células embrionarias y tumorales. Las primeras empiezan a moverse para ir formando tejidos y órganos. Las segundas adquieren movilidad para emigrar a otros órganos y, una vez allí, se detienen para anidar y formar los tumores secundarios, las metástasis. Un proceso, por tanto, que es crucial en las primerísimas fases de la vida, pero que también está presente cuando las células cancerosas se diseminan.
Nieto, académica de la Real Academia de Ciencias y Premio Nacional de Investigación, lidera un equipo de 20 personas en el Instituto de Neurociencias de Alicante (IN-CSIC-UMH), centro mixto del CSIC y la Universidad Miguel Hernández, acreditado como Centro de Excelencia Severo Ochoa.
Pregunta: ¿La metástasis es el gran reto en el tratamiento del cáncer?
Respuesta: Efectivamente, la metástasis es la responsable de más del 90% de las muertes por cáncer.
P: Su investigación se centra en desentrañar los mecanismos de ese proceso: la diseminación de células cancerosas del tumor primario a otras partes del cuerpo.
R: Sí, es uno de nuestros temas. Durante décadas, la investigación del cáncer se ha centrado en el tumor primario. Gracias a ese trabajo se han logrado progresos en la supervivencia de los pacientes. Pero es evidente que también hay que fijarse en la etapa en la que las células cancerosas se diseminan desde el tumor primario y colonizan órganos distantes. En el grupo llevamos más de 25 años trabajando sobre la idea de que, en la progresión del cáncer hacia la metástasis, hay una activación aberrante de genes embrionarios.
P: ¿En qué consiste esa activación y qué consecuencias tiene?
R: Hace años descubrimos unos genes fundamentales para el desarrollo del embrión porque dotan a las células de capacidad de movimiento. Esto tiene sentido porque durante el desarrollo embrionario, muchas células nacen lejos de su destino final, así que activan esos genes y se desplazan al lugar donde deben realizar su función. Algo así se produce en la diseminación de las células cancerosas.
P: Es un juego de activación y desactivación.
R: Usaré una metáfora basada en interruptores. En el desarrollo embrionario, este proceso se basa en un grupo de genes que se encargan de dotar de movimiento a las células; entonces están encendidos, y eso es esencial para el progreso del embrión. Cuando las células llegan a su destino, estos genes se apagan y normalmente permanecen apagados durante la vida del adulto sano. Sin embargo, en algunas patologías como el cáncer vuelven a encenderse. Y van a hacer lo mismo que hacían en el embrión, pero ahora, en lugar de ser un proceso beneficioso, es deletéreo porque consiguen diseminar células del tumor primario a otros órganos. Cuando llegan, anidan y forman las metástasis.
P: Ahora que se conoce la reactivación de esos programas embrionarios y su relación con la metástasis, ¿hacia dónde debe dirigirse la investigación?
R: Por un lado, hay que seguir estudiando los tumores primarios, sobre todo la heterogeneidad celular. Las células de un tumor no son todas iguales, incluso se pueden encargar de distintas funciones. Y los tumores evolucionan, adquieren nuevas mutaciones que modifican su malignidad. Pero, además, ahora hay que poner el foco en el análisis del nicho metastásico: el entorno que las células diseminadas por la activación de los genes embrionarios van a colonizar.
P: ¿Por qué es importante el concepto de plasticidad celular?
R: La plasticidad celular es el cambio de comportamiento de las células a lo largo de un proceso, bien sea el desarrollo embrionario o la progresión tumoral. Cuando hallamos la conexión entre el desarrollo embrionario y el cáncer, y vimos que estos genes se activan en el tumor primario para que las células se diseminen, lo primero que pensamos –incluidas las farmacéuticas– era que había que encontrar una forma de impedir esa activación o inhibirla. Así prevendríamos la metástasis. Con los años vimos que no era tan sencillo. Creíamos que el desprendimiento de células del tumor primario ocurría en etapas avanzadas del cáncer. Hoy sabemos que ocurre desde fases tempranas, y, de hecho, en el momento del diagnóstico, la mayoría de los pacientes, si no todos, ya tienen células diseminadas que se han desprendido.
R: Es decir, ¿puede haberse iniciado la metástasis antes de la detección del tumor primario?
R: La metástasis no siempre, porque eso ya implica la formación de tumores secundarios, y muchos pacientes son diagnosticados antes de su aparición, pero sí la cascada de eventos que terminará por dar lugar a las metástasis. Sabemos que las células del tumor primario adquieren capacidad de moverse. A este proceso se le denomina transición epitelio-mesénquima [EMT]. Pero la célula mesenquimática [móvil] se transforma otra vez en epitelial [estática] cuando anida en otro órgano. Esta es la transición inversa, mesénquima-epitelio, que forma la metástasis. Cuando ya existen células tumorales en el torrente sanguíneo y diseminadas en otros órganos, si bloqueamos estos genes del programa embrionario, detendremos los movimientos celulares; eso sería bueno para impedir que se diseminen más células del tumor primario, pero puede hacer que las ya diseminadas aniden mejor y formen metástasis. Puede ser contraproducente.

Células tras sufrir la transición epitelio-mesénquima, que da movilidad a la células_IN
P: ¿Qué hacer entonces?
R: Centrarnos en otras estrategias: 1) En lugar de inhibir el proceso de la EMT, hay que encontrar las susceptibilidades específicas de las células que ya han sufrido la transición para matarlas selectivamente, y 2) Estudiar qué ocurre en los órganos distantes y cuál es el ambiente favorable que hay ahí –el nicho metastásico– para anularlo y lograr que, aunque las células lleguen, no puedan anidar.
P: ¿Habría que entender qué señales se envían desde esos órganos distantes para atraer a las células que llegan del tumor primario?
R: Más bien qué señales hay en el nicho metastásico. Curiosamente, las células tumorales envían unas vesiculitas –exosomas– que llevan información y educan a los órganos distantes para generar el nicho metastásico, como si preparasen un nido. Tenemos que seguir investigando para conocerlo mejor y averiguar cuáles son las señales que instruyen a las células cancerosas para formar las metástasis.
P: Usted señala que hay que entender mejor las susceptibilidades de las células que están sufriendo la transición y emigrando.
R: Sí, para eliminarlas antes de que aniden o bien lograr que cuando lleguen no sean capaces de anidar. Al principio queríamos impedir esa transición epitelio-mesénquima para que las células no salieran del tumor. Pero como decía antes, seguramente llegaríamos tarde y, si ya hubiera células diseminadas, podrían formar metástasis más fácilmente.
P: Cuando alude a los genes de los programas embrionarios, ¿se refiere a los genes Snail que descubrió su equipo hace tiempo?
R: Hace años descubrimos los genes Snail [caracol] en vertebrados y comprobamos que su activación dotaba a las células de movimiento. Son genes tan importantes para el desarrollo embrionario que cuando están defectuosos, el embrión se detiene. Con el tiempo se ha visto que, además de los genes Snail, hay otros genes que también ayudan a las células a desplazarse. Para que las células se desprendan tienen que separarse de sus vecinas, y para ello reprimen las moléculas que las mantienen unidas; también activan los genes asociados con el comportamiento migratorio y tienen impacto en el citoesqueleto, que hace que las células cambien de forma para moverse; influyen en la división celular… Además, las células que han sufrido la epitelio-mesénquima son muy resistentes a casi todo lo que puede inducir la muerte celular. Esto tiene mucho sentido desde la perspectiva del desarrollo embrionario, porque esas células tienen que ser resistentes para llegar a su destino.
P: Y también tiene mucho que ver con el cáncer.
R: Exacto, porque lamentablemente, también las hace más resistentes a la quimioterapia, la radioterapia e incluso la inmunoterapia, que es el último gran avance en terapias oncológicas.
P: Parece una contradicción que la reactivación de programas embrionarios que son clave para la vida también esté en la base de enfermedades mortales como el cáncer.
R: Así es, parece una contradicción, pero en realidad nos explica la riqueza de la biología. Las células tumorales utilizan en su propio beneficio mecanismos que estaban disponibles en la naturaleza. Para el progreso del cáncer, este necesita diseminarse; es exactamente el mismo concepto biológico que se da en el embrión, que al principio tiene muy pocas células y al final muchísimas, y uno de los mecanismos que utiliza es la diseminación celular. Estas, cuando llegan a su destino, se dividen y forman los órganos correspondientes. Por eso es tan importante volver siempre al embrión. Ahí están implementadas todas las funciones de estos genes; cuanto más las entendamos, mejor atacaremos a las células tumorales.
P: En las últimas décadas se han producido grandes avances en los tratamientos contra el cáncer. ¿Cuál diría que es el gran reto de la ciencia para luchar contra esta enfermedad?
R: Creo que el desafío es impedir la formación de metástasis o ser capaces de tratarlas lo antes posible. Pero el cáncer no es una enfermedad, sino cientos de ellas con distintas características. De hecho, hay algunos tipos de cáncer como el de mama que hace 20 o 30 años tenía una supervivencia baja y ahora un porcentaje altísimo de mujeres sobreviven a él. Otros tipos de tumores como el cáncer de páncreas o el melanoma siguen siendo de mal pronóstico, pero la llegada de la inmunoterapia ha sido un hito para los tratamientos. Y de nuevo, impedir que se formen las metástasis es el gran reto.
P: ¿Las terapias futuras se dirigirán a la desactivación de la metástasis? ¿Se trataría de evitar esos mecanismos que la posibilitan?
R: Sí y no. No se trataría de evitar el movimiento de las células porque, como decía, llegaríamos tarde. Hay que centrarse en lo que sucede en los órganos distantes, en ese nicho metastásico, y entender el microambiente del tumor, lo que hay alrededor del mismo y las interacciones que se producen entre las células tumorales y las normales. Todo esto puede influir positiva o negativamente en la progresión del cáncer. Estas interacciones tienen un gran impacto en la formación de las metástasis, y además, se están viendo muchos mecanismos de regulación cruzada entre la plasticidad celular y la respuesta del sistema inmune, lo que afecta a la eficacia de la inmunoterapia. Todo está entrelazado y, como sucede hasta ahora, lo que mejor funcionará serán los tratamientos combinados para atacar el cáncer desde distintas vertientes.

Metástasis cerebral de melanoma en rató_IN
P: ¿Existe algún tratamiento experimental que trate no de bloquear, sino de regular esos cambios de comportamiento celular y evitar que las células tumorales aniden en otros órganos?
R: Todavía no. Muchos laboratorios farmacéuticos y centros de investigación estaban desarrollado inhibidores para evitar la transición epitelio-mesénquima, pero no se han usado porque, como he explicado, podrían ser contraproducentes. Aún no existe ninguna terapia, pero hay hallazgos experimentales importantes para eliminar selectivamente las células que han sufrido una transición epitelio-mesénquima o incluso tratar de convertirlas en otro tipo de células que no sean dañinas para el paciente.
P: Su grupo trabaja en otras enfermedades como la fibrosis.
R: Sí, trabajamos en enfermedades degenerativas asociadas al envejecimiento para promover terapias que ayuden a la reparación de órganos. En la degeneración de órganos, como en la fibrosis, las células que estaban funcionando bien pierden mecanismos de regulación, se activan estos genes de forma aberrante y empiezan a degenerar. Al final, la degeneración de tejidos puede dar lugar al fallo del órgano y con ello a la muerte del paciente. El envejecimiento es, en gran parte, el declive del buen funcionamiento. El deterioro es causado tanto por procesos biológicos intrínsecos como por agentes externos, y va ocurriendo a lo largo de la vida. Con el tiempo se van acumulando daños celulares que provocan el deterioro de la función, y parte de ese deterioro es también la activación de los genes embrionarios. En este caso se encienden los interruptores de aquellos genes que deberían estar apagados y al revés, se apagan algunos que deberían estar encendidos. Esto es debido a que, en respuesta al daño, se activan mecanismos que tratan de reparar el tejido, pero a veces el daño es crónico y al no poderse reparar, el tejido degenera. Sabemos que en los procesos degenerativos fibróticos se activan los genes embrionarios, y también que, si los apagamos de nuevo, la enfermedad se atenúa.
P: ¿Qué otras investigaciones se realizan en el Instituto de Neurociencias?
R: Es importante que el IN tenga también visibilidad como centro de investigación del cáncer. Pero aún más, hay que visibilizar la investigación en el cáncer que se realiza en el CSIC en general porque se conoce poco. Existen muchos grupos trabajando en centros de toda España. El CIC de Salamanca es de referencia, pero nuestro Instituto, el IIB Alberto Sols en Madrid, el IBBTEC en Cantabria, el IBMB en Barcelona, el CABIMER en Sevilla y otros contribuyen con trabajos excelentes. Hay que crear una red de los grupos de investigación que trabajan en cáncer, una especie de instituto virtual, tal y como se recoge en el Libro Blanco del CSIC.
Mónica Lara del Vigo / CSIC Comunicación
Comparte esto:
- Haz clic para compartir en WhatsApp (Se abre en una ventana nueva)
- Haz clic para compartir en Facebook (Se abre en una ventana nueva)
- Haz clic para compartir en Twitter (Se abre en una ventana nueva)
- Haz clic para enviar un enlace por correo electrónico a un amigo (Se abre en una ventana nueva)
- Haz clic para compartir en Telegram (Se abre en una ventana nueva)
- Haz clic para compartir en LinkedIn (Se abre en una ventana nueva)
Relacionado
Te podría gustar
Salud y Bienestar
Mounjaro: qué es, cómo funciona y por qué es el nuevo fármaco estrella contra la obesidad
Publicado
hace 21 horasen
7 abril, 2026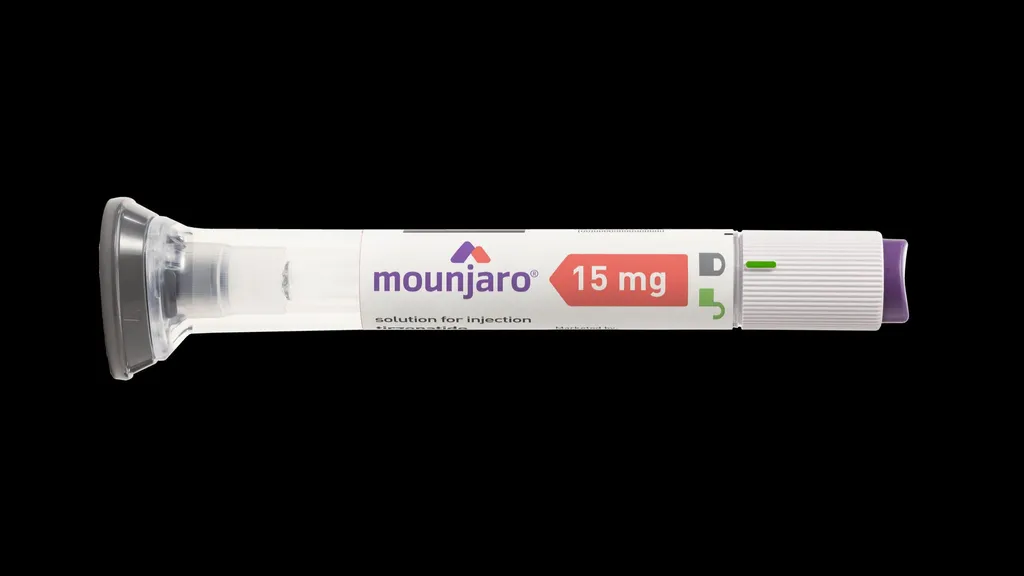
La lucha contra la obesidad ha dado un giro en los últimos años gracias al desarrollo de nuevos medicamentos que van más allá de las dietas y el ejercicio. Uno de los fármacos más prometedores en este campo es Mounjaro, cuyo principio activo es la tirzepatida. Desarrollado por la farmacéutica Eli Lilly, este medicamento se perfila como uno de los tratamientos más eficaces para la pérdida de peso sostenida en personas con obesidad o sobrepeso, incluso en aquellas que han fracasado con métodos tradicionales.
¿Qué es Mounjaro y cómo actúa en el organismo?
Mounjaro es un medicamento inyectable de administración semanal que combina dos mecanismos de acción en uno: actúa sobre los receptores del péptido similar al glucagón tipo 1 (GLP-1) y del polipéptido insulinotrópico dependiente de glucosa (GIP). Esta doble acción potencia su eficacia frente a otros fármacos ya existentes como Ozempic o Wegovy, que solo se centran en el GLP-1.
Estos receptores están implicados en el control del apetito, la regulación del azúcar en sangre y el metabolismo. Al activarlos, Mounjaro logra:
-
Reducir el apetito y aumentar la sensación de saciedad.
-
Retrasar el vaciado gástrico, lo que prolonga la sensación de estar lleno.
-
Mejorar la sensibilidad a la insulina, reduciendo los niveles de glucosa en sangre.
-
Favorecer la pérdida de grasa corporal mientras preserva la masa muscular.
Aprobación y uso médico
Mounjaro fue aprobado inicialmente en Estados Unidos por la FDA en 2022 como tratamiento para la diabetes tipo 2. Sin embargo, su eficacia para la pérdida de peso ha sido tan destacada que en noviembre de 2023 también recibió la aprobación para su uso como medicamento contra la obesidad en personas con un índice de masa corporal (IMC) superior a 30 o superior a 27 en casos con enfermedades asociadas como hipertensión o apnea del sueño.
En Europa, la Agencia Europea del Medicamento (EMA) ya ha dado luz verde a su comercialización como tratamiento para la diabetes tipo 2, y se espera que en 2025 se amplíe su indicación para la obesidad. En España, de momento solo se dispensa en hospitales bajo prescripción médica, y su uso para adelgazar aún no está cubierto por la sanidad pública.
Eficacia comprobada: ¿cuánto peso se puede perder con Mounjaro?
Los estudios clínicos muestran que Mounjaro puede generar una pérdida de peso superior al 20% del peso corporal en algunos pacientes. En el ensayo clínico SURMOUNT-1, en el que participaron más de 2.500 adultos con obesidad o sobrepeso, los resultados fueron espectaculares:
-
Los pacientes tratados con tirzepatida en su dosis más alta (15 mg) perdieron una media del 22,5% de su peso corporal tras 72 semanas de tratamiento.
-
Un 36% de los participantes perdió más del 25% de su peso, un porcentaje que hasta ahora solo era posible con cirugía bariátrica.
-
Los efectos beneficiosos sobre la presión arterial, el colesterol y la resistencia a la insulina también fueron significativos.
Estas cifras colocan a Mounjaro en la cima de los tratamientos farmacológicos contra la obesidad, superando con creces a medicamentos como Saxenda (liraglutida) o Wegovy (semaglutida).
¿Para quién está indicado Mounjaro?
Aunque ha ganado popularidad como medicamento para adelgazar, Mounjaro no es un fármaco de uso cosmético. Está destinado a personas con obesidad diagnosticada o con sobrepeso severo que ya presentan riesgos para la salud. Sus indicaciones médicas incluyen:
-
Personas con un IMC ≥30 (obesidad).
-
Personas con un IMC ≥27 que tengan alguna comorbilidad como hipertensión, dislipemia o diabetes tipo 2.
-
Pacientes con obesidad resistente a dieta, ejercicio y otros tratamientos médicos.
No se recomienda para personas con un peso saludable, ni como tratamiento exclusivo sin acompañamiento médico o sin cambios en el estilo de vida.
¿Cómo se administra?
Mounjaro se presenta en forma de pluma precargada para inyección subcutánea, que el paciente puede administrarse una vez a la semana en el abdomen, el muslo o la parte superior del brazo.
El tratamiento comienza con una dosis baja que se va aumentando progresivamente para minimizar los efectos secundarios, especialmente los gastrointestinales. El esquema típico de dosis es:
-
2,5 mg/semana durante 4 semanas (fase inicial).
-
Incremento gradual hasta 5, 10 o incluso 15 mg/semana (fase de mantenimiento), dependiendo de la tolerancia y los objetivos del paciente.
Efectos secundarios y precauciones
Como cualquier medicamento, Mounjaro no está exento de efectos adversos. Los más comunes están relacionados con el sistema digestivo:
-
Náuseas
-
Vómitos
-
Diarrea o estreñimiento
-
Dolor abdominal
Estos síntomas suelen ser leves y temporales, especialmente durante las primeras semanas. Sin embargo, hay que vigilar posibles reacciones más graves, como:
-
Pancreatitis aguda
-
Hipoglucemia (en pacientes con diabetes tratados también con insulina o sulfonilureas)
-
Posibles efectos sobre la tiroides (en estudios con animales)
Mounjaro está contraindicado en personas con antecedentes de cáncer medular de tiroides o síndrome de neoplasia endocrina múltiple tipo 2. También se desaconseja en embarazadas, mujeres lactantes y menores de edad.
¿Cuánto cuesta Mounjaro?
Uno de los principales inconvenientes de Mounjaro es su precio. En Estados Unidos, el coste mensual ronda los 1.000 dólares sin seguro médico. En Europa, su precio puede variar, pero se espera que se sitúe entre los 250 y 400 euros al mes, según dosis y país. En España, al no estar aún autorizado como tratamiento para la obesidad, su dispensación está restringida y no cuenta con financiación pública.
¿Es el “nuevo Ozempic”?
A menudo se compara Mounjaro con otros medicamentos similares como Ozempic o Wegovy, ambos basados en semaglutida. La principal diferencia es que Mounjaro combina dos hormonas intestinales (GLP-1 y GIP), lo que potencia su eficacia para perder peso.
Además, los estudios demuestran que la pérdida de peso con Mounjaro es superior: entre un 15% y un 22% en función de la dosis, frente al 10-15% que suele lograrse con semaglutida.
Perspectivas de futuro
Mounjaro es solo la punta del iceberg en una nueva generación de medicamentos diseñados para combatir la obesidad como una enfermedad crónica, no como un problema estético. Su impacto podría ser comparable al que tuvo en su día la insulina para la diabetes o las estatinas para el colesterol.
Se espera que en los próximos años surjan más combinaciones de hormonas intestinales que mejoren aún más los resultados. Además, las farmacéuticas trabajan ya en versiones orales para facilitar su uso.
Conclusión
Mounjaro se ha consolidado como una de las terapias más eficaces y revolucionarias contra la obesidad. Su doble mecanismo de acción, sus resultados clínicos espectaculares y su potencial para cambiar el abordaje del sobrepeso lo convierten en una herramienta de primer orden para los profesionales de la salud.
No obstante, debe utilizarse bajo control médico, con seguimiento profesional y acompañado de cambios en los hábitos de vida. No es una solución mágica, pero sí una aliada poderosa en el camino hacia un peso saludable y una mejor calidad de vida.
Puedes seguir toda la actualidad visitando Official Press o en nuestras redes sociales: Facebook, Twitter o Instagram.
Comparte esto:
- Haz clic para compartir en WhatsApp (Se abre en una ventana nueva)
- Haz clic para compartir en Facebook (Se abre en una ventana nueva)
- Haz clic para compartir en Twitter (Se abre en una ventana nueva)
- Haz clic para enviar un enlace por correo electrónico a un amigo (Se abre en una ventana nueva)
- Haz clic para compartir en Telegram (Se abre en una ventana nueva)
- Haz clic para compartir en LinkedIn (Se abre en una ventana nueva)








Tienes que estar registrado para comentar Acceder