Salud y Bienestar
Describen de dónde vienen los antojos en el embarazo
Publicado
hace 2 añosen

SINC – OFFICIAL PRESS
¿De dónde vienen los antojos en el embarazo? Un estudio en hembras de ratón muestra que la gestación induce una reorganización de los circuitos neuronales relacionados con la motivación y el deseo que impulsan a comer productos dulces y calóricos. Estos caprichos muy recurrentes y en exceso pueden deteriorar la salud metabólica, cognitiva y psicológica de la descendencia. Se desconoce aún si estos resultados son extrapolables a los humanos.
Describen los mecanismos neuronales responsables de los antojos en el embarazo
Todo el mundo ha experimentado alguna vez el deseo repentino e incontrolable de comer un alimento determinado. Estos impulsos, conocidos como antojos, son muy comunes, sobre todo durante el embarazo.
En esta etapa, el organismo materno experimenta una serie de cambios fisiológicos y de comportamiento con el fin de crear un entorno favorable para el desarrollo del embrión. Sin embargo, el consumo frecuente de alimentos sabrosos y calóricos, derivado de estos caprichos, contribuye al aumento de peso y a la obesidad gestacional, hecho que puede acarrear consecuencias negativas para la salud del bebé.
“Existen muchos mitos y creencias populares en torno a los antojos, aunque los mecanismos neuronales responsables de su aparición son poco conocidos”, explica Marc Claret, líder del grupo de Control neuronal del metabolismo del Instituto de Investigación Biomédica August Pi i Sunyer (IDIBAPS).
Claret lidera, junto a Roberta Haddad-Tóvolli, investigadora de su grupo, un estudio que aporta nuevas evidencias sobre las alteraciones de la actividad neuronal que dan lugar a dichos caprichos. El trabajo, publicado en la revista Nature Metabolism, se ha realizado en hembras de ratón.

Los autores del estudio publicado en Nature Metabolism, Roberta Haddad-Tóvolli y Marc Claret. / IDIBAPS
Reorganización de los circuitos neuronales
De acuerdo con los resultados de la investigación, durante el embarazo el cerebro de estas roedoras experimenta cambios en las conexiones funcionales de los circuitos de recompensa, así como de los centros gustativos y sensoriomotores. Además, al igual que las mujeres embarazadas, las hembras de ratón son más sensibles a los dulces y desarrollan conductas de ingesta compulsiva de alimentos calóricos.
Gracias a este modelo, los investigadores descubrieron que durante la gestación hay una remodelación de varios circuitos neuronales y, en particular, cambios en el sistema dopaminérgico de la recompensa –que proporciona placer ante estímulos concretos como, por ejemplo, un alimento muy tentador–.
“La alteración de estas estructuras nos llevó a explorar la vía mesolímbica, una de las rutas de transmisión de señales de las neuronas dopaminérgicas. La dopamina es un neurotransmisor clave en los comportamientos de motivación o deseo”, comenta Claret.
Los investigadores observaron que los niveles de dopamina, así como la actividad de su receptor D2R, aumentaban en el núcleo accumbens −una región cerebral implicada en el circuito de recompensa−. “Este hallazgo sugiere que el embarazo induce una reorganización completa de los circuitos neuronales mesolímbicos, a través de las neuronas DR2”, señala Haddad-Tóvolli.
“Asimismo, estas células neuronales y su alteración también serían las responsables de la aparición de los antojos, ya que la ansiedad por la comida, típica del embarazo, desapareció después de bloquear su actividad”, añade la experta.
Efecto en la descendencia
Por último, demostraron que los antojos persistentes tienen consecuencias para la descendencia. En concreto, afectan a su metabolismo, así como al desarrollo de los circuitos neuronales que regulan la ingesta de alimentos, lo que conlleva un aumento del peso corporal, ansiedad y trastornos alimentarios.
No sabemos si los resultados son extrapolables a los humanos. Pero recomendamos moderar los antojos durante la gestación para minimizar posibles efectos negativos
“La mayoría de los estudios se centran en analizar cómo los hábitos permanentes de la madre, como la obesidad, la desnutrición o el estrés crónico, afectan a la salud del bebé. Sin embargo, nuestro trabajo indica que basta con conductas cortas pero recurrentes, como los antojos, para aumentar la vulnerabilidad psicológica y metabólica de la descendencia”, afirma Claret.
Las conclusiones podrían contribuir a mejorar las guías clínicas nutricionales para embarazadas, a fin de asegurar una adecuada nutrición prenatal y prevenir la aparición de enfermedades.
“Actualmente no sabemos si estos resultados observados en el modelo de ratón son extrapolables a los humanos. Pero, en cualquier caso, recomendaríamos moderar los episodios de antojos durante la gestación para minimizar posibles efectos negativos sobre la descendencia”, concluye el experto.
Referencia:
Haddad-Tóvolli et al. “Food craving-like episodes during pregnancy are mediated by accumbal dopaminergic circuits”. Nature Metabolism. Doi: 10.1038/s42255-022-00557-1.
Comparte esto:
- Haz clic para compartir en WhatsApp (Se abre en una ventana nueva)
- Haz clic para compartir en Facebook (Se abre en una ventana nueva)
- Haz clic para compartir en Twitter (Se abre en una ventana nueva)
- Haz clic para enviar un enlace por correo electrónico a un amigo (Se abre en una ventana nueva)
- Haz clic para compartir en Telegram (Se abre en una ventana nueva)
- Haz clic para compartir en LinkedIn (Se abre en una ventana nueva)
Relacionado
Salud y Bienestar
Mounjaro: qué es, cómo funciona y por qué es el nuevo fármaco estrella contra la obesidad
Publicado
hace 14 horasen
7 abril, 2026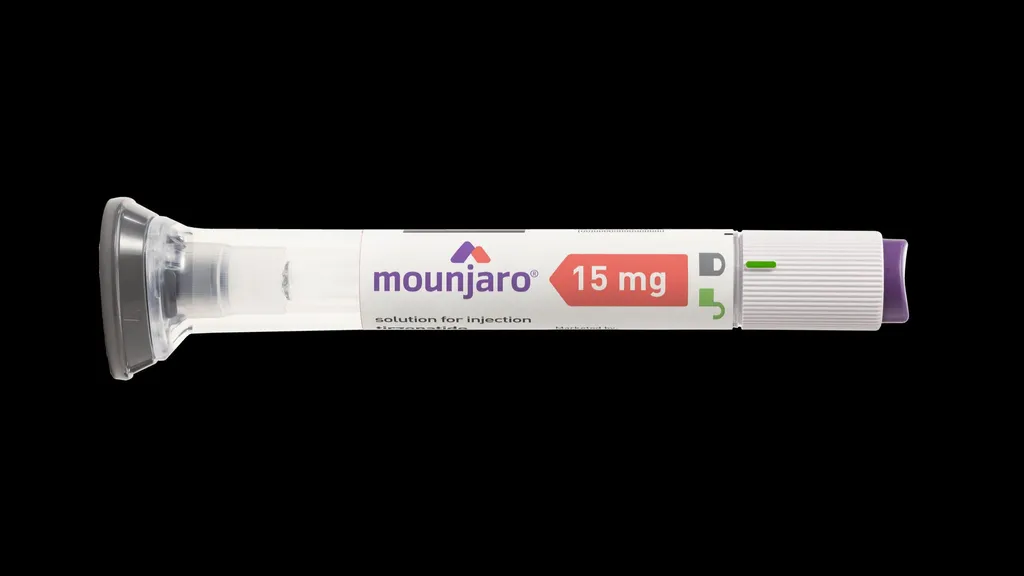
La lucha contra la obesidad ha dado un giro en los últimos años gracias al desarrollo de nuevos medicamentos que van más allá de las dietas y el ejercicio. Uno de los fármacos más prometedores en este campo es Mounjaro, cuyo principio activo es la tirzepatida. Desarrollado por la farmacéutica Eli Lilly, este medicamento se perfila como uno de los tratamientos más eficaces para la pérdida de peso sostenida en personas con obesidad o sobrepeso, incluso en aquellas que han fracasado con métodos tradicionales.
¿Qué es Mounjaro y cómo actúa en el organismo?
Mounjaro es un medicamento inyectable de administración semanal que combina dos mecanismos de acción en uno: actúa sobre los receptores del péptido similar al glucagón tipo 1 (GLP-1) y del polipéptido insulinotrópico dependiente de glucosa (GIP). Esta doble acción potencia su eficacia frente a otros fármacos ya existentes como Ozempic o Wegovy, que solo se centran en el GLP-1.
Estos receptores están implicados en el control del apetito, la regulación del azúcar en sangre y el metabolismo. Al activarlos, Mounjaro logra:
-
Reducir el apetito y aumentar la sensación de saciedad.
-
Retrasar el vaciado gástrico, lo que prolonga la sensación de estar lleno.
-
Mejorar la sensibilidad a la insulina, reduciendo los niveles de glucosa en sangre.
-
Favorecer la pérdida de grasa corporal mientras preserva la masa muscular.
Aprobación y uso médico
Mounjaro fue aprobado inicialmente en Estados Unidos por la FDA en 2022 como tratamiento para la diabetes tipo 2. Sin embargo, su eficacia para la pérdida de peso ha sido tan destacada que en noviembre de 2023 también recibió la aprobación para su uso como medicamento contra la obesidad en personas con un índice de masa corporal (IMC) superior a 30 o superior a 27 en casos con enfermedades asociadas como hipertensión o apnea del sueño.
En Europa, la Agencia Europea del Medicamento (EMA) ya ha dado luz verde a su comercialización como tratamiento para la diabetes tipo 2, y se espera que en 2025 se amplíe su indicación para la obesidad. En España, de momento solo se dispensa en hospitales bajo prescripción médica, y su uso para adelgazar aún no está cubierto por la sanidad pública.
Eficacia comprobada: ¿cuánto peso se puede perder con Mounjaro?
Los estudios clínicos muestran que Mounjaro puede generar una pérdida de peso superior al 20% del peso corporal en algunos pacientes. En el ensayo clínico SURMOUNT-1, en el que participaron más de 2.500 adultos con obesidad o sobrepeso, los resultados fueron espectaculares:
-
Los pacientes tratados con tirzepatida en su dosis más alta (15 mg) perdieron una media del 22,5% de su peso corporal tras 72 semanas de tratamiento.
-
Un 36% de los participantes perdió más del 25% de su peso, un porcentaje que hasta ahora solo era posible con cirugía bariátrica.
-
Los efectos beneficiosos sobre la presión arterial, el colesterol y la resistencia a la insulina también fueron significativos.
Estas cifras colocan a Mounjaro en la cima de los tratamientos farmacológicos contra la obesidad, superando con creces a medicamentos como Saxenda (liraglutida) o Wegovy (semaglutida).
¿Para quién está indicado Mounjaro?
Aunque ha ganado popularidad como medicamento para adelgazar, Mounjaro no es un fármaco de uso cosmético. Está destinado a personas con obesidad diagnosticada o con sobrepeso severo que ya presentan riesgos para la salud. Sus indicaciones médicas incluyen:
-
Personas con un IMC ≥30 (obesidad).
-
Personas con un IMC ≥27 que tengan alguna comorbilidad como hipertensión, dislipemia o diabetes tipo 2.
-
Pacientes con obesidad resistente a dieta, ejercicio y otros tratamientos médicos.
No se recomienda para personas con un peso saludable, ni como tratamiento exclusivo sin acompañamiento médico o sin cambios en el estilo de vida.
¿Cómo se administra?
Mounjaro se presenta en forma de pluma precargada para inyección subcutánea, que el paciente puede administrarse una vez a la semana en el abdomen, el muslo o la parte superior del brazo.
El tratamiento comienza con una dosis baja que se va aumentando progresivamente para minimizar los efectos secundarios, especialmente los gastrointestinales. El esquema típico de dosis es:
-
2,5 mg/semana durante 4 semanas (fase inicial).
-
Incremento gradual hasta 5, 10 o incluso 15 mg/semana (fase de mantenimiento), dependiendo de la tolerancia y los objetivos del paciente.
Efectos secundarios y precauciones
Como cualquier medicamento, Mounjaro no está exento de efectos adversos. Los más comunes están relacionados con el sistema digestivo:
-
Náuseas
-
Vómitos
-
Diarrea o estreñimiento
-
Dolor abdominal
Estos síntomas suelen ser leves y temporales, especialmente durante las primeras semanas. Sin embargo, hay que vigilar posibles reacciones más graves, como:
-
Pancreatitis aguda
-
Hipoglucemia (en pacientes con diabetes tratados también con insulina o sulfonilureas)
-
Posibles efectos sobre la tiroides (en estudios con animales)
Mounjaro está contraindicado en personas con antecedentes de cáncer medular de tiroides o síndrome de neoplasia endocrina múltiple tipo 2. También se desaconseja en embarazadas, mujeres lactantes y menores de edad.
¿Cuánto cuesta Mounjaro?
Uno de los principales inconvenientes de Mounjaro es su precio. En Estados Unidos, el coste mensual ronda los 1.000 dólares sin seguro médico. En Europa, su precio puede variar, pero se espera que se sitúe entre los 250 y 400 euros al mes, según dosis y país. En España, al no estar aún autorizado como tratamiento para la obesidad, su dispensación está restringida y no cuenta con financiación pública.
¿Es el “nuevo Ozempic”?
A menudo se compara Mounjaro con otros medicamentos similares como Ozempic o Wegovy, ambos basados en semaglutida. La principal diferencia es que Mounjaro combina dos hormonas intestinales (GLP-1 y GIP), lo que potencia su eficacia para perder peso.
Además, los estudios demuestran que la pérdida de peso con Mounjaro es superior: entre un 15% y un 22% en función de la dosis, frente al 10-15% que suele lograrse con semaglutida.
Perspectivas de futuro
Mounjaro es solo la punta del iceberg en una nueva generación de medicamentos diseñados para combatir la obesidad como una enfermedad crónica, no como un problema estético. Su impacto podría ser comparable al que tuvo en su día la insulina para la diabetes o las estatinas para el colesterol.
Se espera que en los próximos años surjan más combinaciones de hormonas intestinales que mejoren aún más los resultados. Además, las farmacéuticas trabajan ya en versiones orales para facilitar su uso.
Conclusión
Mounjaro se ha consolidado como una de las terapias más eficaces y revolucionarias contra la obesidad. Su doble mecanismo de acción, sus resultados clínicos espectaculares y su potencial para cambiar el abordaje del sobrepeso lo convierten en una herramienta de primer orden para los profesionales de la salud.
No obstante, debe utilizarse bajo control médico, con seguimiento profesional y acompañado de cambios en los hábitos de vida. No es una solución mágica, pero sí una aliada poderosa en el camino hacia un peso saludable y una mejor calidad de vida.
Puedes seguir toda la actualidad visitando Official Press o en nuestras redes sociales: Facebook, Twitter o Instagram.
Comparte esto:
- Haz clic para compartir en WhatsApp (Se abre en una ventana nueva)
- Haz clic para compartir en Facebook (Se abre en una ventana nueva)
- Haz clic para compartir en Twitter (Se abre en una ventana nueva)
- Haz clic para enviar un enlace por correo electrónico a un amigo (Se abre en una ventana nueva)
- Haz clic para compartir en Telegram (Se abre en una ventana nueva)
- Haz clic para compartir en LinkedIn (Se abre en una ventana nueva)









Tienes que estar registrado para comentar Acceder